[Quipu Issue Paper] Variation study Ⅱ - SNP(Single Nucleotide Polymorphism) Analysis
- Posted at 2010/02/17 14:37
- Filed under 생물정보
연재 순서
1. Assembly
2. Variation study
3. Expression study
4. Epigenomics
5. Genome Annotation
6. Next Generation Bioinformatics
7. Data Management for web 2.0 Era
8. Semantic Network for Integrated Biology Data
9. Gene Network Discovery by Text-mining
10. Centralization for High-throughput Data Analysis
이번 연재에서는 Next Generation Sequencing의 첫 번째 Application인 Variation study 중에 SNP(Single Nucleotide Polymorphism) 분석법에 대해 알아보도록 하겠습니다.
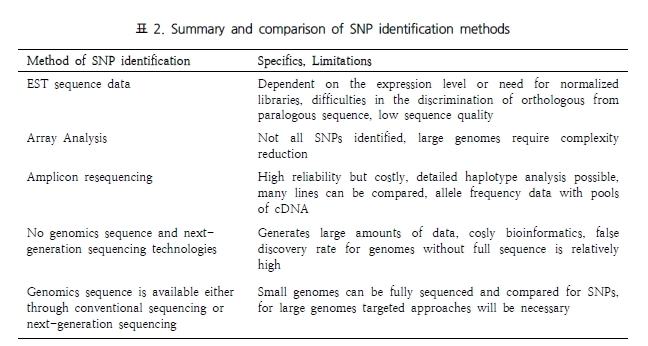
인간 유전체 상에 가장 많이 존재하는 형태의 다형성은 유전체상의 특정 염기서열 하나의 변화이며, 흔히 SNP(Single Nucleotide Polymorphism) 또는 단일염기다형성이라고 부른다. 한 논문에서는 SNP를 검출하는 방법을 다섯 가지로 요약해 나타냈다(표 2)[3]. 이러한 방법들의 공통된 특징은 유전자 또는 염색체 부위를 증폭한 산물에 대한 염기서열을 분석하고 여러 염기서열을 정렬하여 염기서열 차이로서 SNP 존재 여부를 확인하는 것이다. 이러한 관점으로 볼 때 정렬되는 서열이 많을수록 통계적으로도 안정적이며 명확한 variation을 분석할 수 있게 된다. 따라서 제한된 시간 동안 가장 많은 서열을 생산할 수 있는 NGS는 이에 가장 부합하는 분석 도구가 될 것이다.
또한 HapMap project에서 발표한 human 유전체의 SNP 분포를 확인해 보면 공개된 SNP의 약 34.1%에 해당하는 SNP가 30bp 안에 군집하여 분포한다는 것이다(그림 2)[8]. 이는 종전의 마이크로어레이 방식에서 NGS 방식의 SNP 탐색으로의 전환이 매우 필수적임을 시사한다. 그 이유는 마이크로어레이에 심어질 프로브 서열 내에 또 다른 SNP가 포함될 가능성이 매우 높으며 이러한 SNP는 고정되어 있는 프로브 서열로 인해 탐색이 되지 않는 치명적인 제한점을 NGS 방식의 시퀀싱을 통해 매우 효율적으로 해결할 수 있기 때문이다.
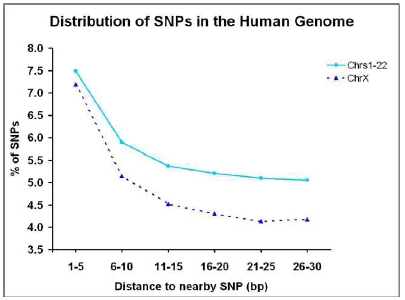 그림 2. Human Genome의 SNP 분포.
그림 2. Human Genome의 SNP 분포.
30bp 내에 많은 SNP이 군집을 이루며 모여 있다.
1. Assembly
2. Variation study
3. Expression study
4. Epigenomics
5. Genome Annotation
6. Next Generation Bioinformatics
7. Data Management for web 2.0 Era
8. Semantic Network for Integrated Biology Data
9. Gene Network Discovery by Text-mining
10. Centralization for High-throughput Data Analysis
이번 연재에서는 Next Generation Sequencing의 첫 번째 Application인 Variation study 중에 SNP(Single Nucleotide Polymorphism) 분석법에 대해 알아보도록 하겠습니다.
2-1-1. SNP (Single Nucleotide Polymorphism) Analysis
인간 유전체 상에 가장 많이 존재하는 형태의 다형성은 유전체상의 특정 염기서열 하나의 변화이며, 흔히 SNP(Single Nucleotide Polymorphism) 또는 단일염기다형성이라고 부른다. 한 논문에서는 SNP를 검출하는 방법을 다섯 가지로 요약해 나타냈다(표 2)[3]. 이러한 방법들의 공통된 특징은 유전자 또는 염색체 부위를 증폭한 산물에 대한 염기서열을 분석하고 여러 염기서열을 정렬하여 염기서열 차이로서 SNP 존재 여부를 확인하는 것이다. 이러한 관점으로 볼 때 정렬되는 서열이 많을수록 통계적으로도 안정적이며 명확한 variation을 분석할 수 있게 된다. 따라서 제한된 시간 동안 가장 많은 서열을 생산할 수 있는 NGS는 이에 가장 부합하는 분석 도구가 될 것이다.

또한 HapMap project에서 발표한 human 유전체의 SNP 분포를 확인해 보면 공개된 SNP의 약 34.1%에 해당하는 SNP가 30bp 안에 군집하여 분포한다는 것이다(그림 2)[8]. 이는 종전의 마이크로어레이 방식에서 NGS 방식의 SNP 탐색으로의 전환이 매우 필수적임을 시사한다. 그 이유는 마이크로어레이에 심어질 프로브 서열 내에 또 다른 SNP가 포함될 가능성이 매우 높으며 이러한 SNP는 고정되어 있는 프로브 서열로 인해 탐색이 되지 않는 치명적인 제한점을 NGS 방식의 시퀀싱을 통해 매우 효율적으로 해결할 수 있기 때문이다.

30bp 내에 많은 SNP이 군집을 이루며 모여 있다.
Variation 분석에 적합하도록 시퀀싱이 수행되고 나면 실제 많은 reads를 이용한assembly가 수행되고 그 결과를 바탕으로 서열을 비교하여 variation 부분을 탐색하게 된다. 그 중 SNP 분석의 경우, 시퀀싱 중에 일어난 오류에 기인한 mis-match인지 variation으로 인한 mismatch 인지를 구별하기 위한 여러 가지 파라미터를 설정하게 된다. Mismatch frequency 및 coverage(해당 위치의 서열 coverage)를 중심으로 잠재적인 SNP를 선별하게 된다. 이때, 조금 더 정확한 SNP를 구별하기 위해 viewer를 통해 서열 퀄리티를 확인하는 경우도 발생하게 되는데, 다양한 플랫폼에서 생성된 reads들은 고유의 포맷을 유지하고 있고 대부분의 open source로 제공되는 프로그램들은 특정 플랫폼의 데이터만을 다루도록 하고 있어 이를 확인하기에는 어려움이 따른다. 또한 특정 SNP가 cSNP 인지 여부나 더 나아가 단백질 서열까지 변화되는 synonymous SNP 인지 여부를 판단하기에는 생물정보학자의 도움이 절실히 요구된다. 그러나 이러한 과정 모두를 해결해 줄 수 있는 프로그램들이 계속해서 개발되어지고 있다. 그 중 CLC NGS Cell과 CLC Genomics Workbench는 NGS 데이터의 assembly와 사용자 편의의 인터페이스를 통해 분석된 SNP의 아미노산 서열 변화 확인을 위한 translation 분석, SNP 검증을 위한 PCR 프라이머 디자인, in-silico 클로닝 등의 통합 분석을 생물정보 전문가가 아닌 일반 연구자들 스스로 진행할 수 있도록 하고 있다. 뿐만 아니라 assembly를 수행할 때 reference 서열을 이미 annotation이 완료된 ‘.gbk’ 데이터로 진행할 수 있어, SNP로 생각되는 유전자의 위치 및 이미 등록된 SNP 정보들까지도 표시하여 함께 확인할 수 있기 때문에 NGS 기술을 이용한 SNP 분석에 추천할 만한 분석 파이프라인이라고 하겠다(그림 3).
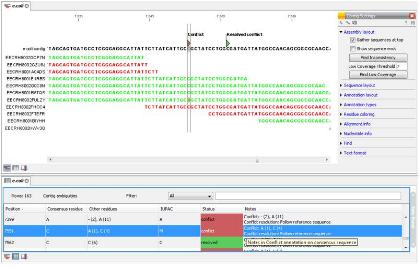 그림 3. SNP 탐색을 위한 CLC Genomics Workbench
그림 3. SNP 탐색을 위한 CLC Genomics Workbench

다음 연재에서는 SNP(Single Nucleotide Polymorphism) 이외에 정상 표현형인 인간의 유전체에 존재하면서 유전적 다양성에 기여하고, 암 또는 많은 질병 감수성과도 연관될 가능성이 높은 유전자 복제수(Copy number) 변이 분석법에 대해 알아보도록 하겠습니다. 많은 관심 부탁드립니다.
참고문헌
참고문헌
1. 이종극 (2006) 질병유전체분석법(Genetic Variation and Diseases)
2. Eck SH, Benet-Pagès A, Flisikowski K, Meitinger T, Fries R, Strom TM. (2009) Whole genome sequencing of a single Bos taurus animal for single nucleotide polymorphism discovery. Genome Biol. 10(8), R82.
3. Ganal MW, Altmann T, Röder MS. (2009) SNP identification in crop plants. Curr Opin Plant Biol. 2, 211-217
4. Xie C, Tammi MT. (2009) CNV-seq, a new method to detect copy number variation using high-throughput sequencing. BMC Bioinformatics. 10, 80
5. Illumina : SNP Genotyping and CNV Analysis
(http://www.illumina.com/documents/products/datasheets/datasheet_genomic_sequence.pdf)
6. Bentley DR. et al. (2008) Accurate whole human genome sequencing using reversible terminator chemistry. Nature. 2008 456, 53-59
7. Ng SB. et al. (2009) Targeted capture and massively parallel sequencing of 12 human exomes. Nature. 461, 272-276
8. Koboldt DC, Miller RD, Kwok PY. (2006) Distribution of human SNPs and its effect on high-throughput genotyping. Hum Mutat. 3, 249-254.
9. 박종화 (2009) 변이체학을 위한 생정보학 분석도구. Medical POSTGRADUATES. 3(37), 131-133
10. 유향숙, 김선영 (2009) Variome 국제연구동향. Medical POSTGRADUATES. 3(37), 134-137
2. Eck SH, Benet-Pagès A, Flisikowski K, Meitinger T, Fries R, Strom TM. (2009) Whole genome sequencing of a single Bos taurus animal for single nucleotide polymorphism discovery. Genome Biol. 10(8), R82.
3. Ganal MW, Altmann T, Röder MS. (2009) SNP identification in crop plants. Curr Opin Plant Biol. 2, 211-217
4. Xie C, Tammi MT. (2009) CNV-seq, a new method to detect copy number variation using high-throughput sequencing. BMC Bioinformatics. 10, 80
5. Illumina : SNP Genotyping and CNV Analysis
(http://www.illumina.com/documents/products/datasheets/datasheet_genomic_sequence.pdf)
6. Bentley DR. et al. (2008) Accurate whole human genome sequencing using reversible terminator chemistry. Nature. 2008 456, 53-59
7. Ng SB. et al. (2009) Targeted capture and massively parallel sequencing of 12 human exomes. Nature. 461, 272-276
8. Koboldt DC, Miller RD, Kwok PY. (2006) Distribution of human SNPs and its effect on high-throughput genotyping. Hum Mutat. 3, 249-254.
9. 박종화 (2009) 변이체학을 위한 생정보학 분석도구. Medical POSTGRADUATES. 3(37), 131-133
10. 유향숙, 김선영 (2009) Variome 국제연구동향. Medical POSTGRADUATES. 3(37), 134-137
11. 임선희, 정연준. (2009) 새로운 유전체 변이의 등장 : 유전자 복제수 변이. Medical POSTGRADUATES. 3(37), 149-153
Posted by 人Co
- Tag
- CNV, cSNP, HapMap project, NGS, SNP, variation, 단일염기다형성, 생물정보학, 염기서열, 유전자 복제수 변이, 인실리코젠
- Response
- No Trackback , No Comment
- RSS :
- https://post-blog.insilicogen.com/blog/rss/response/41
Trackback URL : 이 글에는 트랙백을 보낼 수 없습니다


